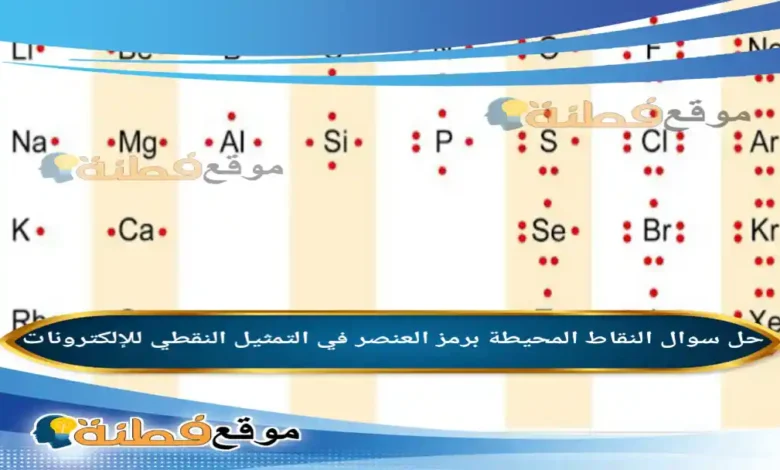
حل سوال النقاط المحيطة برمز العنصر في التمثيل النقطي للإلكترونات، برز تساؤل مهم حول الرموز والنقاط التي تحيط بها، والتي تُستخدم لتبسيط فهم بنية الذرات. يتساءل الطلاب بشكل متكرر عن معنى هذه النقاط وكيفية تحديد عددها وأهميتها في التفاعلات الكيميائية. يُعتبر فهم هذا التمثيل البصري أساسيًا لإدراك مفهوم الروابط الكيميائية وكيفية تشكُّل الجزيئات والمركبات في هذا المقال عبر موقع فطنة سنقوم بحل سؤال النقاط المحيطة برمز العنصر في التمثيل النقطي للإلكترونات. العديد يتساءل عن ماهيتها الحقيقية وماذا تمثل هذه النقاط تحديدًا في عالم الكيمياء.
من هي النقاط في التمثيل النقطي للإلكترونات
النقاط المحيطة برمز العنصر في “التمثيل النقطي للإلكترونات”، والذي يُعرف علميًا باسم “تركيب لويس” أو “بنية لويس”، هي تمثيل مرئي لإلكترونات التكافؤ. إلكترونات التكافؤ هي الإلكترونات الموجودة في مستوى الطاقة الخارجي للذرة، وهي المسؤولة بشكل أساسي عن تحديد الخصائص الكيميائية للعنصر وكيفية تفاعله مع الذرات الأخرى لتكوين روابط كيميائية.
هذا النموذج البسيط، الذي ابتكره العالم الأمريكي جيلبرت نيوتن لويس، يساعد على تصور كيفية توزيع هذه الإلكترونات الحيوية حول نواة الذرة ومستويات الطاقة الداخلية، والتي يمثلها رمز العنصر الكيميائي، يتم توزيع النقاط حول الرمز لبيان عدد إلكترونات التكافؤ، مما يسهل فهم آلية فقدان أو اكتساب أو مشاركة الإلكترونات أثناء تكوين الروابط الأيونية أو التساهمية.
شاهد أيضاً : بتلاحم واجتماع مجموعة من النقاط يتكون لنا خط فالنقطة هي بداية كل شيء
خصائص التمثيل النقطي للإلكترونات
التمثيل النقطي للإلكترونات، أو تركيب لويس، هو رسم بياني ثنائي الأبعاد يُستخدم في الكيمياء لإظهار الترابط بين ذرات جزيء ما، بالإضافة إلى أزواج الإلكترونات الوحيدة التي قد توجد فيه. تُعد هذه الطريقة أداة أساسية لتمثيل بنية الجزيئات التساهمية والمعقدات.
- الاسم الكامل: تركيب لويس النقطي (Lewis Dot Structure) أو التمثيل النقطي للإلكترونات.
- المكتشف: العالم الكيميائي الأمريكي جيلبرت نيوتن لويس.
- سنة التقديم: اقترح لويس هذا المفهوم لأول مرة في مقالته “الذرة والجزيء” عام 1916.
- الهدف الأساسي: تمثيل إلكترونات التكافؤ لذرة عنصر ما بشكل مرئي وبسيط.
- القاعدة الأساسية: يُكتب رمز العنصر الكيميائي وتُحاط به نقاط، حيث تمثل كل نقطة إلكترون تكافؤ واحد.
- الأهمية: يساعد هذا التمثيل في فهم وتصور كيفية تكوّن الروابط الكيميائية بين الذرات، وتطبيق “قاعدة الثمانيات” التي تنص على ميل الذرات للوصول إلى ثمانية إلكترونات في غلافها الخارجي لتحقيق الاستقرار.
- خطوات الرسم:
- كتابة رمز العنصر.
- تحديد عدد إلكترونات التكافؤ من خلال التوزيع الإلكتروني للعنصر أو موقعه في الجدول الدوري.
- توزيع النقاط (إلكترونات التكافؤ) فرادى على الجوانب الأربعة للرمز أولاً، ثم البدء في عمل أزواج إذا زاد العدد عن أربعة.
وفيما يدور حول سوال النقاط المحيطة برمز العنصر في التمثيل النقطي للإلكترونات الجواب الصحيح هو إلكترونات التكافؤ التي تشارك في تكوين الروابط الكيميائية. يمكن القول إن النقاط المحيطة برمز العنصر في تمثيل لويس هي لغة بصرية مبسطة وفعالة في عالم الكيمياء. لقد سهّلت هذه الطريقة على الطلاب والعلماء على حد سواء فهم طبيعة إلكترونات التكافؤ ودورها المحوري في تشكيل الروابط بين الذرات، مما يجعلها أداة لا غنى عنها في دراسة بنية المادة وتفاعلاتها.





